近年来,真正让肿瘤免疫治疗重新崛起、目前为业界广泛认可的是两类特异性治疗途径:一种是针对免疫检查点的抗体(CTLA-4、PD-1、PD-L1抑制剂等),另一种是表达嵌合抗原受体的自体T细胞疗法(CAR-T),分别占据了肿瘤免疫疗法的半壁江山。
 tle="点击查看原图" width="630" height="460" border="0" style="width:630px;height:460px;" />
tle="点击查看原图" width="630" height="460" border="0" style="width:630px;height:460px;" />
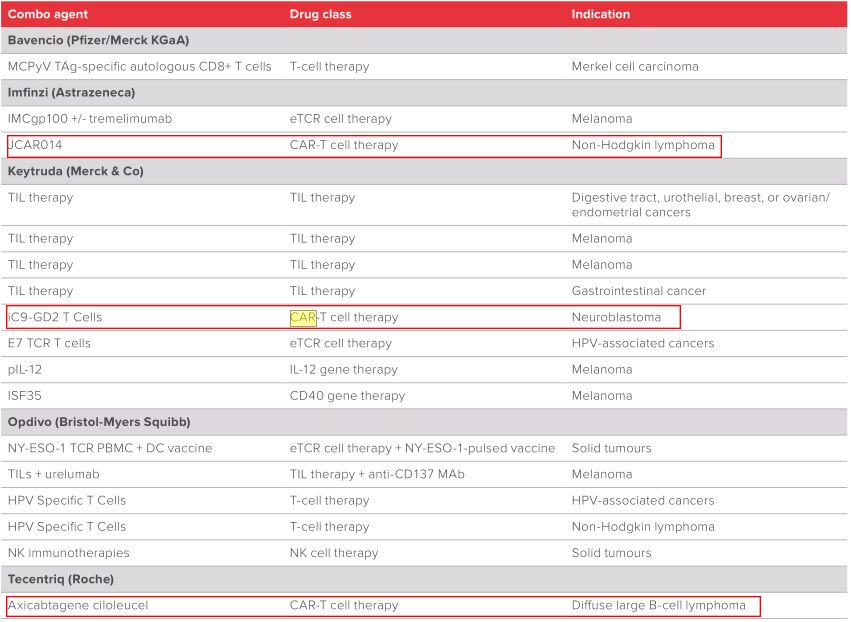
PD-1/PD-L1与细胞疗法或基因疗法联合用药开展的临床研究(图片来源Evaluate)
虽然这两种突破性疗法都是目前肿瘤免疫疗法的热点和投资的风口,但同样面领着单一用药治疗瓶颈。例如CAR-T治疗实体瘤疗效甚微,治疗血液肿瘤仍存在复发的可能性,而PD-1/L1抑制剂包揽的适应症虽多,但总体有效率却很低。随着对肿瘤免疫疗法研究的深入,越来越多的研究机构和公司展开了联合疗法的研究,他们希望能够为极具治疗潜力的免疫疗法找到最佳拍档,以期达到更为理想的治疗效果,让更多的患者从中获益。
而作为CAR-T细胞治疗领域的领军企业,Kite Pharma必然是不会忽略这一布局的,2016年3月,Kite就已经宣布,与罗氏达成合作交易,共同开发CAR-T与PD-L1 抑制剂的联合疗法。
 tle="点击查看原图" width="630" height="217" border="0" style="width:630px;height:217px;" />
tle="点击查看原图" width="630" height="217" border="0" style="width:630px;height:217px;" />
近期,Kite Pharma公布的一项名为ZUMA-6的I/II期临床试验结果(NCT02926833),证明了其anti-CD19 CAR-T细胞产品Yescarta (axi-cel)联合罗氏的PD-L1抑制剂Tecentriq治疗弥漫性大B细胞淋巴瘤(DLBCL)患者安全有效。总体有效率(ORR)为89%(n = 8/9),其中完全缓解率(CR)为56%(n = 5/9)。
入组的包括进展或接受化疗后疾病稳定的,或者是在自体干细胞移植的12个月内,经历疾病进展/复发的难治性DLBCL患者。其中CD-20阳性的肿瘤患者必须接受anti-CD20单克隆抗体的治疗,所有患者都必须先接受蒽环类药物化疗,必须具有0或1的ECOG行为状态。
在研究的第一阶段,9名患者被分成3个队列,所有患者均接受500 mg/m2环磷酰胺和30 mg/m2氟达拉滨的化疗,随后接受2×106/kg剂量的CAR-T细胞输注。细胞输注完成后,3个队列中,患者分别在第21天、第14天和第1天接受Atezolizumab(Tecentriq,PD-L1抑制剂)治疗,且剂量都是相同的:4个剂量,21天1200mg。
其中3个队列的平均年龄为52岁(范围29-66),包括6名男性和3名女性患者。IV期4例,III期2例,II期3例。之前治疗的中位数是3(范围2-4)。关于基线PD-L1状态,用肿瘤细胞/免疫浸润物染色确定以下结果:3 + / 3 +(1例患者),3 + / 2 +(3例患者),2 + / 2 +(1例患者) 0/3 +(1例),样本不可用(3例)。
主要的终点是定义为剂量限制毒性(DLTs)的不良事件(AEs),次要/探索性终点包括ORR、生物标记分析和安全性评价。
临床结果显示,在队列1中,2例患者获得部分缓解(PR),1例患者经历了从PR到CR的转换,获得完全缓解(CR)。队列2中,1例患者CR,1例患者从PR到CR,1例病情稳定。队列3中有2例患者获得CR和1例PR。总体有效率ORR为89%(n=8/9),完全缓解率CR为56%(n=5/9)。
 tle="点击查看原图" />
tle="点击查看原图" />
Frederick L. Locke博士(图片来源 onclive)
Frederick L. Locke博士作为ZUMA-6的主要负责人(同时也是ZUMA-1试验的主要负责人),他指出:“从生物标志物的研究中,我们发现CAR-T细胞与Atezolizumab(Tecentriq,PD-L1抑制剂)联合治疗后,患者外周血中的CAR-T细胞的数量有增加的趋势。
安全性方面,观察到的与CAR-T治疗相关的毒性,和关键的ZUMA-1临床试验相似,即细胞因子释放综合征(CRS)和神经毒性的发生率(Yescarta 基于ZUMA-1的临床结果获批上市)。
9例患者均出现Yescarta(Axi-cel)相关的AE,4例患者出现与Atezolizumab相关的AE。总体而言,8名患者经历了3/4级不良事件,没有出现死亡案例。
在评估安全性时,研究人员试图确定这一联合疗法是否会增加治疗毒性,但结果表明:那些经历严重的CRS和神经毒性的患者在注射Atezolizumab之前发生的。此外,Yescarta (Axi-cel)和Atezolizumab的联合治疗不会导致tocilizumab或类固醇的使用增加(tocilizumab,IL-6R单抗用于对抗患者接受CAR-T治疗后产生的严重或威胁生命的CRS )。
Locke表示,下一步将会扩展到II期临床试验,以确定该联合疗法的安全方案, 一旦确定给药剂量,将会在另外22名患者中进行临床研究,并和在ZUMA-1试验中接受过Yescarta (Axi-cel)单药治疗的DLBCL患者比较治疗效果。
 tle="点击查看原图" width="630" height="178" border="0" style="width:630px;height:178px;" />
tle="点击查看原图" width="630" height="178" border="0" style="width:630px;height:178px;" />
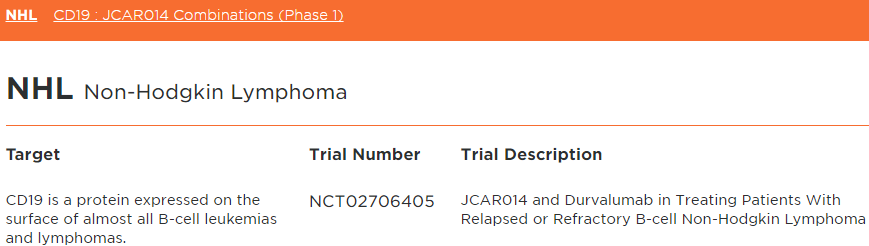
JCAR014联合Durvalumab(图片来源 Juno)
除了以上提起的Kite和罗氏之间共同开展的CAR-T与PD-L1联合用药的临床试验,Juno也与阿斯利康达成了合作协议,共同推进其在研CAR-T细胞产品JCAR014联合后者的PD-L1抑制剂Durvalumab治疗NHL的临床试验(NCT02706405)。
在此,我们期待细胞免疫治疗的先行者,将两种疗法结合在一起开启免疫联合疗法的新篇章,为生物医药研发行业注入新的活力和希望。
来源:医麦客
原标题《Kite携手罗氏上演「双剑合璧」:CAR-T联合PD-L1抑制剂治疗淋巴瘤,总体有效率达89%》





